食品・医薬品・化学物質等の安全性試験
» 受託試験のご案内に戻る
一般毒性試験
食品、医薬品、化学物質等の生体に及ぼす影響を評価する試験です。
短期間または長期間曝露する試験法のほか、発がん性や発がん誘発性の有無を調べる試験法、 光毒性反応を調べる試験法などがあります。
単回投与毒性(急性毒性)試験
目的
試験する医薬品、化学物質、医療材料の抽出液などを動物(マウス、ラットなど)に、口や静脈、皮膚などから1回投与して、 どのような毒性変化が見られるかを明らかにする目的で行います。
動物種
マウスまたはラット
検査項目
一般状態の観察、 体重測定、病理学的検査(肉眼的観察、病理組織学的観察)
反復投与毒性試験
 目的
目的
試験する医薬品、化学物質などを動物に2週間から1年間毎日投与または医療機器を埋植して、どのような毒性変化がどのような程度で見られるかを明らかにします。
投与または埋植期間は被験物質の種類や使用目的、試験目的により決定され、28日間、90日間、6か月間および1年間等があります。 繰り返し投与した場合に認められる変化を種々の手法で観察し、
明らかな毒性変化がみられる用量での、その毒性の種類および程度を明らかにするとともに、 毒性変化が発現しない量(NOAEL)や生体に反応が現れない量(NOEL)を求めます。
動物種
マウス、ラットまたはウサギ
検査項目
一般状態の観察、体重測定、摂餌量、摂水量、尿検査、血液検査(血液学的検査、血液生化学的検査等)、眼科学的検査、
病理学的検査(肉眼的観察、器官重量測定、病理組織学的観察等)
免疫毒性試験
主にアレルギーを調べる試験です。
皮膚感作性試験
代表的な遅延型アレルギーを調べます。Maximization testとAdjuvant and Patch test、 Buehler testが有名。いずれもモルモットに被験物質を数回感作投与した後、惹起を行い、皮膚反応を観察します。
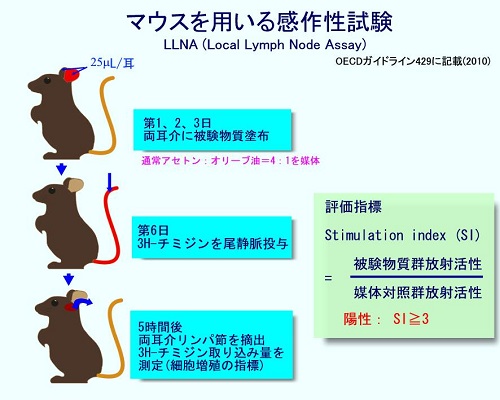
Local Lymph Node Assay (LLNA)
遅延型アレルギーを調べます。
マウスの耳介に被験物質を塗布した後、3H-thymidineを静脈内投与し、所属リンパ節でリンパ球の増殖が活発になっているかどうかを調べるます。
遺伝毒性試験
細菌を用いる遺伝毒性試験(in vitro試験系)
細菌を用いる復帰突然変異試験(Ames試験)
検定菌
サルモネラ菌株および大腸菌株
目的
被験物質の遺伝子突然変異誘発性の有無について調べます。汎用されている遺伝毒性試験の1つで、各種ガイドラインに記載され、実施が義務付けられています。
各検定菌が形成する復帰変異コロニーの数を調べます。
細菌を用いるumu試験
検定菌
サルモネラ菌株
目的
被験物質のDNA損傷性の有無について調べます。被験物質がアミノ酸を含み、Ames試験で判定が困難な場合に実施される試験の1つで、
市販のキットを用いて試験を実施します。処理液を吸光度計で測定し、色の変化の有無を調べます。
培養細胞を用いる遺伝毒性試験(In vitro試験系)
培養細胞を用いる染色体異常試験
使用細胞
チャイニーズ・ハムスター細胞株、ヒト末梢リンパ球など
目的
被験物質の染色体構造異常、数的異常誘発性の有無について調べます。
汎用されている遺伝毒性試験の1つです。各種ガイドラインに記載され、実施が義務付けられています。細胞分裂中期像を観察することにより、 被験物質の染色体構造異常誘発性と数的異常誘発性を調べます。
動物を用いる遺伝毒性試験(in vivo試験系)
げっ歯類を用いる小核試験
動物種
マウスあるいはラット
目的
被験物質の生体内における染色体異常誘発性の有無について調べます。汎用されている遺伝毒性試験の1つです。各種ガイドラインに記載され、実施が義務付けられています。
骨髄、末梢血、皮膚(表皮)、 舌(表皮)、肝臓などの細胞を用いて実施され、小核を有する細胞の出現率を調べます。
トランスジェニックマウスを用いる遺伝毒性試験
動物種
トランスジェニックマウス
目的
被験物質の生体内における遺伝子突然変異誘発性の有無について調べます。In vitroあるいはin vivo試験系の遺伝毒性試験において陽性結果が得られた場合、
生体内における遺伝毒性を確認するために実施されます。 ゲノムDNAが抽出できる臓器を用いて実施され、宿主菌が形成するコロニーの表現形あるいはプラーク形成の有無を調べます。
多臓器不定期DNA合成試験
動物種
ウサギ、ラットあるいはマウス
目的
被験物質の生体内におけるDNA損傷性の有無について調べます。生体内における遺伝毒性を確認するために実施されます。組織切片が作製可能な臓器であれば、
試験の実施が可能。標的臓器について包埋切片のオートラジオグラフ標本を作製したのち、光学顕微鏡により観察します。 各細胞の核内に取り込まれるラジオアイソトープ(トリチウム)の量を調べます。
局所刺激性試験
局所刺激性試験は、医薬品、化学物質等が生体組織と接触した場合、その局所に対してどのような影響を与えるかを評価するための試験です。
眼刺激性試験
目的
被験物質の眼組織に対する組織障害性、炎症誘起性または刺激性について調べます。臨床での使用方法で被験物質が眼組織に接触する場合の組織障害を検出する試験です。
点眼方法および試験期間は臨床での使用方法を考慮して設定します。 評価は暴露部位の肉眼的観察をもとに行います。
使用動物種
ウサギ
口腔粘膜刺激性試験
目的
被験物質の口腔粘膜に対する組織障害性、炎症誘起性または刺激性について調べます。臨床での使用方法で被験物質が口腔粘膜組織に接触する場合の組織障害を検出する試験です。
適用方法および試験期間は臨床での使用方法を考慮して設定します。 評価は曝露部位の肉眼的観察および病理学的検査をもとに行います。
使用動物種
ハムスター
腟粘膜刺激性試験
目的
被験物質の腟粘膜に対する組織障害性、炎症誘起性または刺激性について調べます。臨床での使用方法で被験物質が腟粘膜に接触する場合の組織障害を検出する試験です。
適用方法および試験期間は臨床での使用方法を考慮して設定します。 評価は暴露部位の肉眼的観察および病理学的検査をもとに行います。
使用動物種
ウサギ
皮膚刺激性試験
目的
被験物質の皮膚に対する組織障害性、炎症誘起性または刺激性について調べます。臨床での使用方法で被験物質が皮膚に接触する場合の皮膚組織障害を検出する試験です。
適用方法および試験期間は臨床での使用方法を考慮して設定します。 評価は暴露部位の肉眼的観察をもとに行います。
使用動物種
ウサギ
皮内反応試験
目的
被験物質の皮内に対する組織障害性、炎症誘起性または刺激性について調べます。臨床での使用方法で被験物質が生体内に接触する場合の皮膚組織障害を検出する試験です。
評価は暴露部位の肉眼的検査をもとに行います。
使用動物種
ウサギ
その他、各種刺激性試験
陰茎刺激性試験、直腸粘膜刺激性試験などがあります。





